научное издание МГТУ им. Н.Э. Баумана
НАУКА и ОБРАЗОВАНИЕ
Издатель ФГБОУ ВПО "МГТУ им. Н.Э. Баумана". Эл № ФС 77 - 48211. ISSN 1994-0408
# 10, октябрь 2011
УДК 57.087
Введение
В современной онкоцитологии при исследовании материала пункционных биопсий врач-цитолог опирается на качественные признаки, которые носят субъективный характер, поэтому возникают значительные трудности при установлении характера процесса. Так, в настоящее время достоверность цитологического исследования при опухолях и опухолеподобных заболеваниях почек колеблется от 76,4 до 91,3 %. Кроме того, пункция почки является одной из самых сложных, о чем свидетельствует высокий процент неудавшихся пункций (до 11,5 %) [1]. Наибольшие диагностические трудности возникают при дифференциальной цитологической диагностике между реактивными изменениями почечного эпителия (РИ), ангиомиолипомой (АМЛ), и высокодифференцированным почечно-клеточным раком (ВДПКР) [2, 3]. Изображения препаратов, соответствующие наиболее характерной цитологической картине при норме (Н), а также указанных состояниях, приведены на рисунке 1 а-г (препараты предоставлены лабораторией онкоцитологии МНИОИ им. П.А. Герцена).

Рис. 1. Изображения цитологических препаратов почки при
а) норме, б) реактивных изменениях, в) доброкачественных изменениях, г) злокачественных изменениях
В сложных случаях для проведения дифференциальной цитологической диагностики используют окраску азотнокислым серебром (AgNOR), при которой визуализируется внутренняя структура ядер клеток, что позволяет оценить метаболическую и пролиферативную активность клеток. Однако для данного типа окраски в настоящее время не выделены классы ядер клеток, что затрудняет формализацию и объективизацию исследования данных цитологических препаратов [2 -5]. Для повышения эффективности цитологической диагностики опухолей и опухолеподобных заболеваний почек необходимо формализовать численное описание геометрических и текстурных характеристик ядер, алгоритм оценки вероятности диагноза из группы рассматриваемых.
Комплекс морфологических характеристик ядер
Геометрические характеристики ядер. Анализ морфологии ядер клеток почечного эпителия [5] показал, что для оценки морфофункционального состояния клетки, целесообразно ввести следующие геометрические характеристики ядер:
1) Нормированная площадь ядра:
![]()
где ![]() – максимальное значение площади, полученное при обучении алгоритма.
– максимальное значение площади, полученное при обучении алгоритма.
2) Коэффициент округлости ядра:
![]()
где ![]() – периметр ядра.
– периметр ядра.
При стремлении данного коэффициента к 1, форма предмета стремиться к кругу, то есть чем более округлую форму будет иметь анализируемое ядро, тем больший коэффициент ![]() ей будет соответствовать.
ей будет соответствовать.
3) Коэффициент неровности контура ядра:
![]()
Чем меньше этот коэффициент, тем более ровный контур у исследуемого ядра.
Текстурные характеристики ядер. Для оценки морфофункционального состояния клетки, целесообразно использовать следующие текстурные характеристики ядер: равномерность хроматина, количество и размер ядрышек [3, 5].
Для суммарной оценки этих текстурных характеристик был выбран метод матрицы градиентов. Данный метод заключается в построении матрицы, характеризующей вероятность ![]() встречаемости пар точек с яркостями
встречаемости пар точек с яркостями ![]() и
и ![]() на изображении, находящихся в заданном направлении, определяемом углом
на изображении, находящихся в заданном направлении, определяемом углом ![]() = 0, 45, 90, 135, на заданном расстоянии
= 0, 45, 90, 135, на заданном расстоянии ![]() друг от друга. Вычисленная таким образом матрица является квадратной, размера
друг от друга. Вычисленная таким образом матрица является квадратной, размера ![]() , где
, где ![]() – число уровней яркости изображения. В качестве характеристик текстуры используются параметры, вычисляемые по матрице градиентов [5, 6]:
– число уровней яркости изображения. В качестве характеристик текстуры используются параметры, вычисляемые по матрице градиентов [5, 6]:
1) Контраст
![]()
2) Корреляция
![]()
3) Энергия
![]()
4) Гомогенность
![]()
По каждой матрице градиентов вычисляются оценки четырех описанных выше параметров. Для устранения эффекта смещения оценок за счет изменения ориентации клеток на изображениях вычисляются средние значения и максимальный разброс значений параметров в зависимости от угла ![]() для каждого расстояния
для каждого расстояния ![]() . В ходе предварительных исследований было установлено, что текстурные характеристики целесообразно рассчитывать для нескольких значений расстояний
. В ходе предварительных исследований было установлено, что текстурные характеристики целесообразно рассчитывать для нескольких значений расстояний ![]() = {5; 7}, что обусловлено размерами ядерных структур на регистрируемых изображения.
= {5; 7}, что обусловлено размерами ядерных структур на регистрируемых изображения.
Для формирования классов ядер в пространстве признаков необходимо решить задачу кластеризации их в данном пространстве; поэтому на основе сформированного вектора параметров, включившего в себя три геометрических параметра и 16 текстурных, проводилась кластеризация ядер алгоритмом c-средних [6]. В качестве целевой функции данный алгоритм использует сумму квадратов взвешенных отклонений от центров искомых кластеров.
Для определения числа морфофункциональных типов ядер клеток почечного эпителия проводилась оценка качества кластеризации по 2 критериям:
1) Степень однородности кластеров:
![]()
где![]() ,
,
![]() – максимальное количество ядер i-ото кластера, принадлежащее какому-либо одному верифицированному диагнозу,
– максимальное количество ядер i-ото кластера, принадлежащее какому-либо одному верифицированному диагнозу,
![]() – общее число анализируемых ядер.
– общее число анализируемых ядер.
Степень однородности кластеров характеризует наличие в выделенных кластерах ядер, относящихся к разным диагнозам. Значение степени однородности кластера тем выше, чем больше число ядер в кластере, принадлежащих к одному верифицированному диагнозу
2) Степень компактности кластеров:
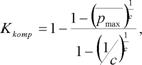
где ![]() – средняя максимальная степень принадлежности ядра к какому-либо кластеру.
– средняя максимальная степень принадлежности ядра к какому-либо кластеру.
Данный коэффициент равен 0, если ![]() , то есть ядро принадлежит всем кластером с одинаковой вероятностью.
, то есть ядро принадлежит всем кластером с одинаковой вероятностью.
Алгоритм вычислительной диагностики
Обобщение результатов классификации отдельных ядер в препарате и вынесение заключения о характере наблюдаемых изменений является задачей вычислительной диагностики (ВД). Вероятностная теория Байеса анализирует вероятности появления отдельных признаков при определенных заболеваниях, относящихся к рассматриваемой группе [7]. Совокупность признаков (S1, S2,… Sp), где p – количество ядер на исследуемом препарате, представляет собой номера кластеров, в которые классифицированы ядра. Далее совокупность признаков Si будем обозначать S. В качестве рассматриваемых диагнозов при дифференциальной диагностике ПКР рассматриваются следующие: D1 – Н, D2 – РИ, D3 – АМЛ, D4 – ВДПКР.
В соответствии с формулой Байеса выражение для апостериорной вероятности P(Dj/S) диагноза Dj при наблюдении признаков S имеет вид:
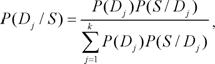
где P(Dj) – априорная вероятность диагноза Dj;
P(S/Dj) – условная вероятность признаков S, т.е. вероятность того, что в случае, если Dj имеет место, то будут обнаружены признаки S;
k– число рассматриваемых диагнозов, k=4.
Сделаем допущение об условной независимости отдельных признаков, т.е., в исследуемом случае, о независимости результатов классификации отдельных ядер с изображения препарата между собой на подмножествах каждого из диагнозов [7]. Введение такого допущения может быть оправдано тем фактом, что материал одной цитологической пробы может содержать ядра, относящиеся к разным классам. Это допущение позволяет выразить совместную вероятность через произведение условных вероятностей каждого из признаков в отдельности:
![]() ,
,
где L– количество кластеров;
Cl – l-й кластер;
pl– число ядер, принадлежащих кластеру Cl;
![]() – условная вероятность того, что при данном диагнозе Dj ядро будет отнесено в кластер Сl.
– условная вероятность того, что при данном диагнозе Dj ядро будет отнесено в кластер Сl.
Таким образом, в предположении равенства априорных вероятностей диагнозов, расчет апостериорной вероятности каждого из диагноза проводится по в соответствии с соотношением:
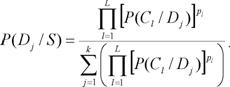
Условные вероятности ![]() оцениваются по обучающей выборке как доля всех ядер, полученных с препаратов с диагнозом Dj, принадлежащих кластеру Cl:
оцениваются по обучающей выборке как доля всех ядер, полученных с препаратов с диагнозом Dj, принадлежащих кластеру Cl:
![]()
где mlj – число ядер, принадлежащих кластеру Cl, и присутствующих на препаратах соответствующих диагнозу Dj;
Nj – общее количество ядер, присутствующих на препаратах соответствующих диагнозу Dj в обучающей выборке.
Решение о рекомендуемом диагнозе Dj принимается по максимуму апостериорной вероятности.
Для определения числа морфофункциональных типов ядер клеток почечного эпителия был проведен их кластерный анализ в сформированном пространстве признаков. Кластеризация проводилась для 120 сегментированных вручную ядер, количество кластеров варьировалось от 4 до 8. Результаты кластеризации оценивались по 2 предложенным критериям, в качестве наилучшего результата кластеризации был выбран случай 5 кластеров (таблица 1), для которого ![]() ,
, ![]() .
.
Таблица 1. Результаты кластеризации для 5 кластеров
Препарат | Число ядер, относящихся к кластеру | Доминирующий кластер | ||||
Кластер №1 | Кластер №2 | Кластер №3 | Кластер №4 | Кластер №5 | ||
Н | 0 | 5 | 0 | 0 | 25 | 5 |
РИ | 0 | 7 | 2 | 21 | 0 | 4 |
АМЛ | 11 | 1 | 16 | 2 | 0 | 1, 3 |
ВД ПКР | 1 | 19 | 2 | 3 | 5 | 2 |
Из таблицы 1 видно, что каждому верифицированному диагнозу соответствует свой морфофункциональный тип ядер клеток. Для АМЛ их выявлено два. Это соответствует медицинским данным о наличии в пробах АМЛ не только ядер эпителиальных клеток, но и ядер миобластов.
Определение качества ВД заболеваний почки проводилось на группе контроля из 30 верифицированных цитологических препаратов. Результаты сравнения верифицированных диагнозов с результатами работы алгоритма ВД представлены в таблице 2.
Таблица 2. Сравнение верифицированных диагнозов с результатами ВД
Верифицированный диагноз | Результаты ВД | ||||
D1 | D2 | D3 | D4 |
| |
D1 (Н) | 6 | 0 | 0 | 1 | 7 |
D2 (РИ) | 0 | 6 | 0 | 1 | 7 |
D3 (АМЛ) | 0 | 0 | 8 | 0 | 8 |
D4 (ВДПКР) | 1 | 0 | 1 | 6 | 8 |
Для 30 препаратов было получено 26 совпадений верифицированного диагноза и результатов ВД (таблица 2), что составляет 86,7%, полученное значение приближается к вероятности постановки правильного диагноза квалифицированным врачом-цитологом.
Выводы
Проведен анализ морфологических параметров ядер клеток почечного эпителия на цитологических препаратах, окрашенных азотнокислым серебром; сформирован комплекс характеристик, включающий три геометрических (площадь, округлость, неровность контура) и 16 текстурных признаков изображений ядер. Текстурные характеристики оцениваются по четырем параметрам полутоновой матрицы градиентов изображения (контраст, корреляция, энергия и гомогенность), для каждого из которых вычисляется среднее значение параметра по четырем направлениям и его максимальный разброс; указанные характеристики вычисляются для двух расстояний между пикселями d=5, 7.
Решена задача формализации морфофункциональных типов ядер. С использованием метода кластеризации с-средних и предложенных в работе критериев оценки качества кластеризации определено число морфофункциональных типов ядер и их численные характеристики. Установлено, что для четырех диагнозов (норма, реактивные изменения, ангиомиолипома, высокодифференцированный почечно-клеточный рак) число морфофункциональных типов равно 5.
Предложен алгоритм вычислительной диагностики, использующий формулу Байеса для расчета апостериорных вероятностей диагнозов из группы рассматриваемых по результатам классификации ядер в цитологическом препарате на сформированные морфофункциональные типы.
В результате экспериментальных исследований на 30 верифицированных препаратах ядер клеток почечного эпителия установлено, что вероятность постановки правильного диагноза составляет 86,7%, что соответствует результатам визуального анализа высококвалифицированным врачом-цитологом.
Созданные в ходе выполнения работы система вычислительной диагностики, методы и алгоритмы анализа изображений цитологических препаратов почечного эпителия могут быть использованы для повышения объективности, снижения трудоемкости цитологического анализа в онкоцитологии, способствовать широкому его распространению в клинико-диагностической практике.
Представленные результаты получены при проведении НИР в рамках реализации ФЦП «Научные и научно-педагогические кадры инновационной России» на 2009 – 2013 годы, ГК № П2276 от 13.11.2009 г. и при поддержке гранта РФФИ 10-08-01310-а.
Литература
1. Злокачественные новообразования в России в 2008 году (заболеваемость и смертность) Под ред. В.И. Чиссова, В.В. Старинского, Г.В. Петровой. – М.: ФГУ МНИОИ им. П.А. Герцена Росздрава, 2010. – 256 с.
- Значение аргентофильных белков областей ядрышковых организаторов в цитологической диагностике рака почки /Волченко Н.Н., Мельникова В.Ю., Спиридонов И.Н. и др. //Российский онкологический журнал. – 2007. – №5. – С.37-39.
- Определение активности областей ядрышковых организаторов при реактивных изменениях почечного эпителия и высокодифференцированном почечно-клеточном раке /Мельникова В.Ю., Спиридонов И.Н., Самородов А.В., Славнова Е.Н. //Современные микроскопические исследования в биологии и медицине: Сб. статей – М.: Лабора, 2006. – С. 153-155.
- Экспрессия аргирофильных белков ядрышкого организатора как показатель степени зрелости доброкачественных и злокачественных опухолей надпочечника /Райхлин Н.Т., Букаева И.А., Баронин А.А. и др. //Архив патологии. – 2002. – № 3. – С.26-30.
- Количественный анализ цитологических изображений почечного эпителия в онкологии /Самородов А. В., Полянская М. Г., Славнова Е. Н. и др. //Биомедицинская радиоэлектроника. – 2007. – №10. – С.21 – 27.
6. Гонсалес Р., Вудс Р. Цифровая обработка изображений. — М.: Техносфера, 2005. – 1072 с.
- Спиридонов И.Н., Самородов А.В. Методы и алгоритмы вычислительной диагностики: Учеб. пособие. – М.: Изд-во МГТУ им. Н.Э. Баумана, 2006. – 50 с.
Публикации с ключевыми словами: вычислительная диагностика, Онкоцитология
Публикации со словами: вычислительная диагностика, Онкоцитология
Смотри также:
Тематические рубрики:
| Авторы |
| Пресс-релизы |
| Библиотека |
| Конференции |
| Выставки |
| О проекте |
| Телефон: +7 (915) 336-07-65 (строго: среда; пятница c 11-00 до 17-00) |
|
||||
| © 2003-2024 «Наука и образование» Перепечатка материалов журнала без согласования с редакцией запрещена Тел.: +7 (915) 336-07-65 (строго: среда; пятница c 11-00 до 17-00) | |||||



